Samenvatting
De variabiliteit in de 24-uurs verzameling van urines is nog steeds een onopgelost probleem ondanks vele studies. De variatie in kreatinine-uitscheiding werd door ons onderzocht in een groep van 270 patiënten waarbij twee direct opeenvolgende 24-uurs urines werden verzameld. Er werden criteria voor de detectie van afwijkende verzamelingen ontwikkeld en getest in deze populatie. De gevonden afwijkingen werden gekwantificeerd, geclassificeerd en de mogelijke oorzaken werden beredeneerd. We hebben aannemelijk gemaakt dat de hoofdoorzaak van de variabiliteit wordt gevormd door verkeerd verzamelen. Ten slotte werden de schriftelijke patiëntinstructies uitgebreid en duidelijker opgeschreven naar aanleiding van de bevindingen in deze studie.
Inleiding
Kreatinine in 24-uurs urine is een maat voor spiermassa en nierfunctie (1,2), maar kent ook andere belangrijke toepassingen, zoals in de endocrinologie de screening op het syndroom van Cushing (cortisoluitscheiding) en feochromocytoom (metanefrines-uitscheiding). Voor beide toepassingen is correcte verzameling van belang; controle hierop is echter moeilijk. De literatuur laat een grote intra-individuele variatie zien in de 24-uurs kreatinine-uitscheiding bij zowel gezonden als bij patiënten (3). Een van de factoren die vaak als oorzaak wordt genoemd is verkeerd verzamelen. De methoden om de volledigheid van verzamelen te controleren, zoals de p-aminobenzoëzuur-excretie en het gebruik van de kreatininecoëfficiënt zijn verre van ideaal, zoals recent is aangetoond (4,5). Hierdoor bestaat er veel scepsis over de bruikbaarheid van de kreatinine-uitscheiding als controle op de correctheid van urine verzamelen. De richtlijn Hypertensie in de tweede en derde lijn beveelt dubbele verzameling aan (NIV-richtlijn Hypertensie) (6), evenals de richtlijn voor het syndroom van Cushing van de Endocrine Society (7). Theoretisch reduceert twee etmalen verzamelen de variatie met wortel √2 (een factor 1,4). Echter, dubbele verzameling geeft geen garantie op volledigheid van verzamelen.
Wil men profiteren van deze reductie in variatie, dan moeten beide verzamelingen correct zijn uitgevoerd. De vergelijking van direct opeenvolgende verzamelingen heeft als voordeel dat langetermijnveranderingen in spiermassa of nierfunctie geen invloed hebben. Ondanks alle gepubliceerde variabiliteit in de kreatinine-uitscheiding blijkt uit de literatuur dat bij goed geïnstrueerde gezonde personen een zeer nauwkeurige verzameling mogelijk is (CV 3,6%) (8). Naar aanleiding hiervan ontstond de vraag om in de eigen patiëntenpopulatie te kijken naar de variatie in de verzameling, hierbij het aantal en de aard van de uitbijters te onderzoeken met als uiteindelijk doel een model te ontwikkelen en dit model als autorisatiemodule in het laboratoriuminformatiesysteem in te bouwen. De gegevens van een dergelijk onderzoek zijn ook nuttig voor het inschatten van schommelingen ten behoeve van laboratoria die ratio’s van uitgescheiden stoffen ten opzichte van kreatinine gebruiken. Bovendien onderzochten we de literatuur op gegevens met betrekking tot de grootte-orde van de storingen door vleesconsumptie, inspanning, menstruatie en kreatinegebruik.
Materiaal en methoden
Patiënten van het Maasstadziekenhuis (Rotterdam) en het Spijkenisse Medisch centrum (Spijkenisse) verzamelden dubbele 24-uurs urines voor routinematig onderzoek. Vrijwel alle verzamelingen vonden plaats bij poliklinische patiënten in het kader van onderzoek naar het syndroom van Cushing, feochromocytoom, carcinoïd (NET), porfyrie, of osteoporose/multipel myeloom bij fractuur. De patiënten werden schriftelijk en mondeling geïnstrueerd om ‘s ochtends vroeg de blaas te legen, de tijd te noteren en vervolgens te verzamelen en de volgende ochtend vroeg om dezelfde tijd de eerste portie bij de verzameling te doen en opnieuw de tijd te noteren. Het volume bij een eventuele licht afwijkende verzameltijd werd mathematisch gecorrigeerd naar de 1440 minuten van een volledig etmaal. Kreatinine in urine werd gemeten met een gecompenseerde Jaffé methode (Dimension VISTA, Siemens Diagnostics, Nederland) of met een enzymatische methode (Cobas 6000, Roche Diagnostics, Nederland), beide gekalibreerd op de referentiewaarden van de SKML. Het volume werd hetzij door weging, hetzij met een maatcylinder bepaald. De patiëntgroep bestond uit 270 patiënten met hypertensie, overgewicht en fracturen. De verschillen in kreatinine-uitscheiding en volume werden berekend door de waarden van het 2e etmaal af te trekken van die van het 1e etmaal. Het percentage verschil werd berekend door het verschil te delen door het gemiddelde van beide etmalen. De data werden geanonimiseerd en prospectief verzameld. De referentiewaarden voor kreatinine-uitscheiding zijn voor mannen 8,0-22,0 mmol/24u en voor vrouwen 6,0-17,0 mmol/24u (9). De referentiewaarden voor het 24-uurs volume zijn 1000-3500 mL/24u (10).
Resultaten
De gegevens van de patiëntenpopulatie zijn weergegeven in Tabel 1.
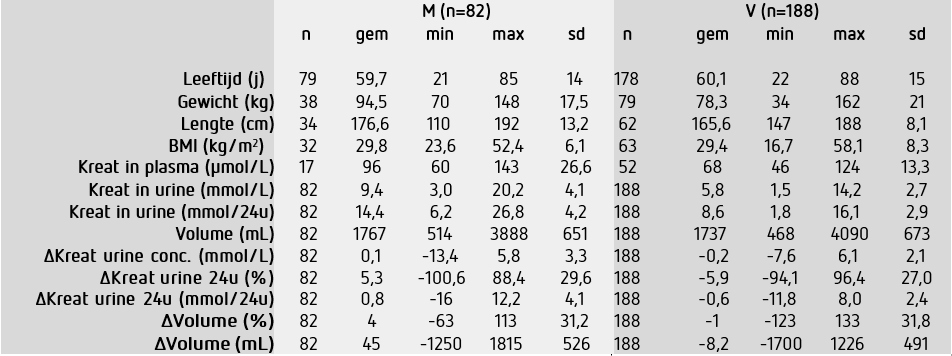
De door een Δ voorafgegane verschillen in variabelen werden bepaald door de waarden in het 2e etmaal van die in het 1e etmaal af te trekken. Niet alle kenmerken waren beschikbaar van alle patiënten.
*N= 270
Keuze van autorisatiegrenzen
De biologische variatie-database van Westgard geeft voor de 24-uurs uitscheiding van kreatinine een intra-individuele variatie van 11% en een tussen-persoonsvariatie van 23% voor gezonden. Hieruit volgt de totale variatiecoëfficiënt als 25% (via de wortel uit de kwadratensom) en dus een spreiding van ± 50%. De gemiddelde uitscheiding in onze totale patiëntengroep is 10,4 mmol/24u. De helft hiervan is circa 5 mmol/24u. Bij 23 van de 270 patiënten bedroeg het verschil tussen beide uitscheidingen meer dan ±5 mmol/24u; deze werden beschouwd als afwijkend en verwijderd. Vervolgens hebben we van deze geschoonde populatie (n = 247) de standaardafwijking berekend (2,0 mmol/24u), waaruit een 95% betrouwbaarheidsinterval van ±4,0 mmol/24u volgt. Dit interval is vervolgens gehanteerd om afwijkende verschillen in kreatinine-uitscheiding tussen het 1e en 2e etmaal op te sporen.
Deze grenzen zijn in overeenstemming met de vroege literatuur waarin een kritisch verschil in kreatinine-uitscheiding van 3,5 mmol/24u voor vrouwen en 4,3 mmol/24u voor mannen wordt vermeld. Deze werden overigens bepaald in een kleine groep gezonden (n = 15) (11). Later is in een uitgebreide studie een kritisch verschil in kreatinine-uitscheiding van 40% als beste keuze aangegeven (12). Dit percentage, toegepast op het eerder vermelde gemiddelde kreatinine-uitscheiding van 10,4 mmol/24u geeft dezelfde ±4,0 mmol/24u op als referentiegrenzen voor het verschil in kreatinine-uitscheiding. Referentiegrenzen voor het verschil in 24-uurs volume als percentage zijn reeds beschreven in de literatuur (13). Deze auteurs berekenden een kritisch verschil van 54,5% in een groep van 459 gezonden. Wij hebben in ons verder onderzoek deze referentiegrenzen overgenomen als ± 55%.
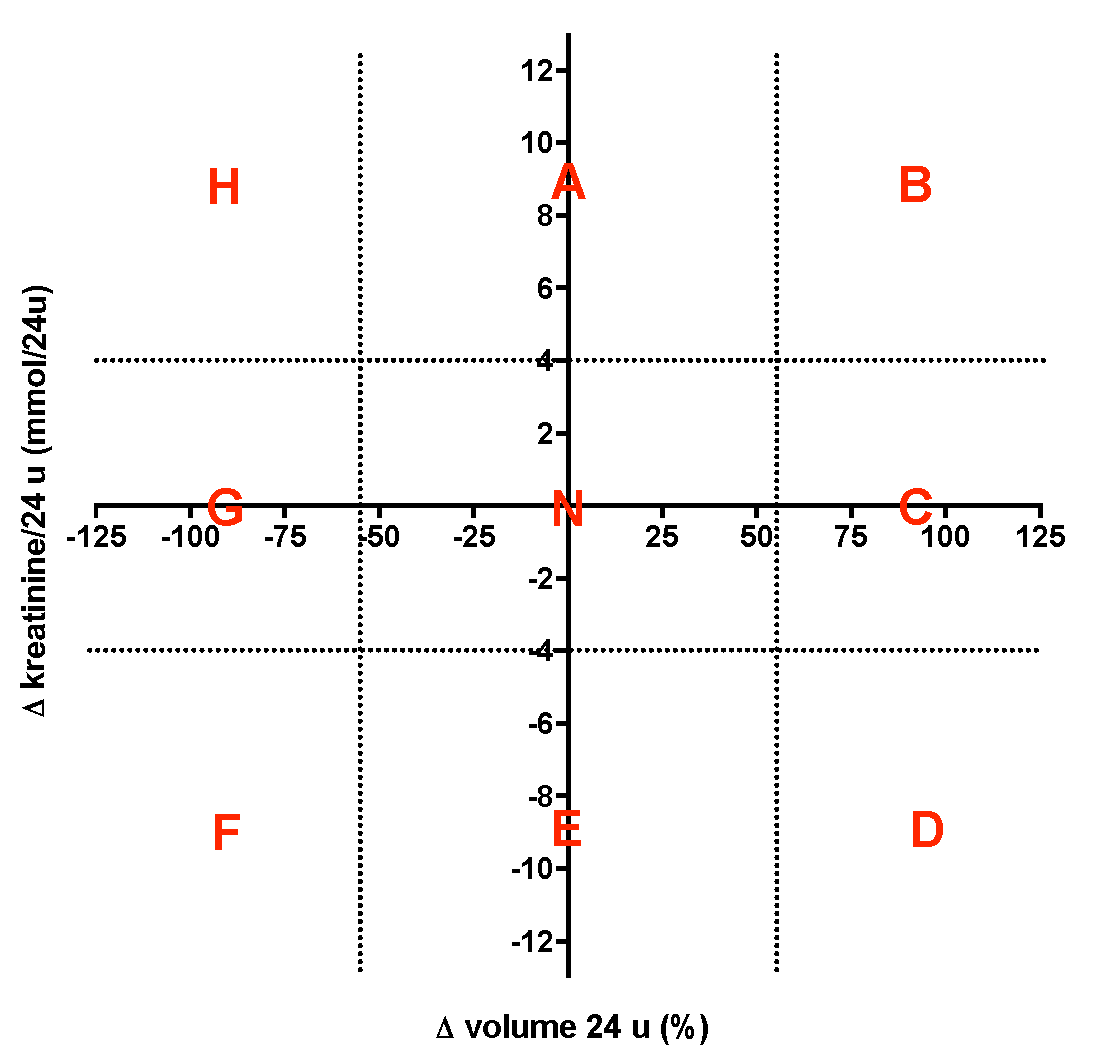
Figuur 1. Verschil in volume als percentage uitgezet tegen het verschil in kreatinine-uitscheiding als mmol/24u. De diverse gebieden zijn alfabetisch gecodeerd als: A t/m H zoals weergegeven. N is het normale gebied.
Het volumeverschil als percentage en het verschil in kreatinine-uitscheiding van elke patiënt kunnen gecombineerd in een figuur worden weergegeven (Fig.1). We hebben in deze figuur de verschillende gebieden gecodeerd met een letter (alfabetisch, kloksgewijs, beginnend met A). De gedachte hierbij was dat de “normale” verschillen zich centraal zouden bevinden (gebied N) en de storingen van diverse oorzaak zich als uitbijters in de verschillende gebieden zouden voordoen. Een verschil in kreatinine-uitscheiding geeft overschrijding parallel aan de Y-as, verschil in percentage volume parallel aan de X-as. De tegenover elkaar liggende gebieden A en E, B en F, C en G, D en H zijn complementair omdat de gelijksoortige afwijkingen alleen van teken wisselen. Zo ontstaan afwijkingen in de gebieden C en G uitsluitend door een groot verschil in volume (V1>V2 respectievelijk V2>V1), terwijl het verschil in kreatinine-uitscheiding normaal blijft (verschil in wateruitscheiding, maar correct verzameld). Daarentegen zal een patiënt die vlak voor de tweede dag kreatine slikt in het gebied E kunnen vallen (kreatine wordt afgebroken tot kreatinine).
Er bestaat een beperking bij het hanteren van absolute verschillen in kreatinine-uitscheiding. Wanneer een patiënt een lage kreatinine-uitscheiding heeft (bv. 5 mmol/24u) zullen, bij een verkeerd verzameld volume, de referentiegrenzen van ±4,0 mmol/24u veel moeilijker worden overschreden dan bij een patiënt met hogere kreatinine-uitscheiding (bv. 18 mmol/24u). In onze patiëntenpopulatie komen verschillen buiten ±4,0 mmol/24u niet voor beneden een kreatinine-uitscheiding van 7,4 mmol/24u. Om deze reden hebben we een tweede figuur toegevoegd waarbij op de Y-as het kreatinineverschil niet absoluut (mmol/24u), maar relatief (%) is uitgezet. Beide figuren moeten in gezamenlijke beschouwing de eindconclusie opleveren. In het geschetste geval zal soms een afwijking in het percentageverschil de conclusie afwijkend opleveren, hoewel het verschil in absolute uitscheiding nog normaal is. Gewoonlijk echter stemmen beide signaleringen overeen.
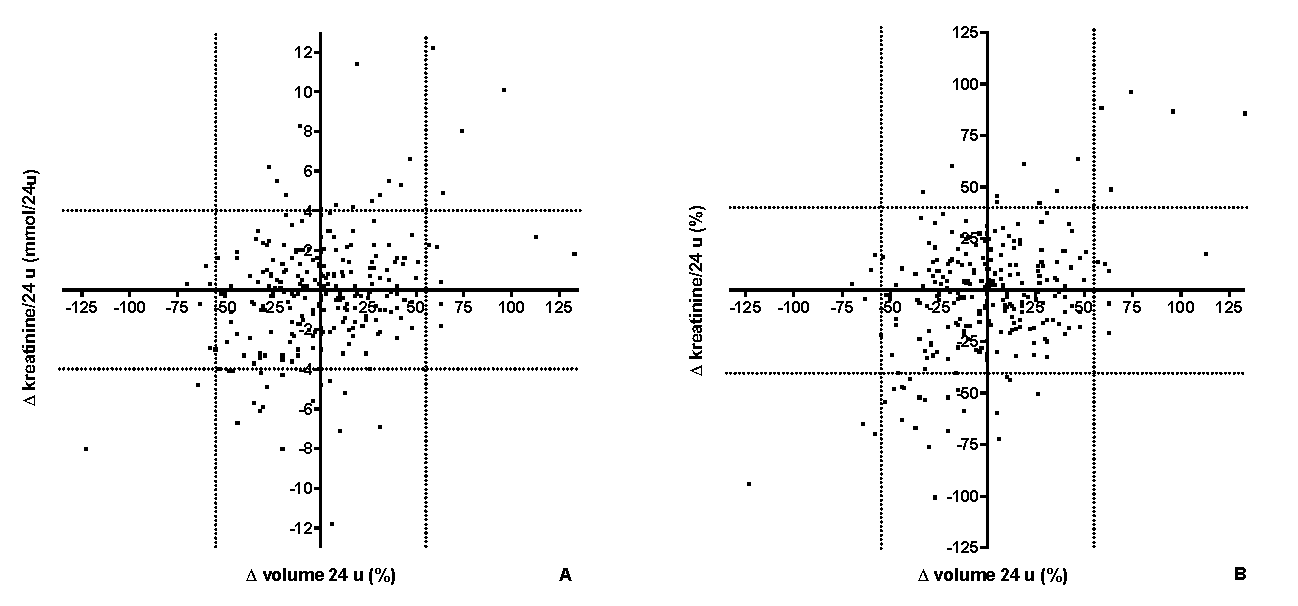
Figuur 2 A) Verschil in volume als percentage uitgezet tegen het verschil in kreatinine-uitscheiding als mmol/24u.
Figuur 2B) Verschil in volume als percentage uitgezet tegen het verschil in kreatinine-uitscheiding als percentage. De gegevens van 270 patiënten zijn uitgezet in beide figuren. De indeling in gebieden in relatie tot de kliniek wordt besproken in de discussie.
Referentiegebied
De verdeling van patiënten in het centrale gebied is tweezijdig symmetrisch: boven de X-as liggen 109, onder de X-as 114, links van de Y-as 103 en rechts van de Y-as 107 patiënten. Deze symmetrie is ook wat men van een referentiegebied zou verwachten. De analytische variatie van de kreatininebepaling (3,2% bij een concentratie van 13,3 mmol/L) draagt maar in zeer geringe mate bij aan de totale variatie binnen het referentiegebied.
Uitbijters
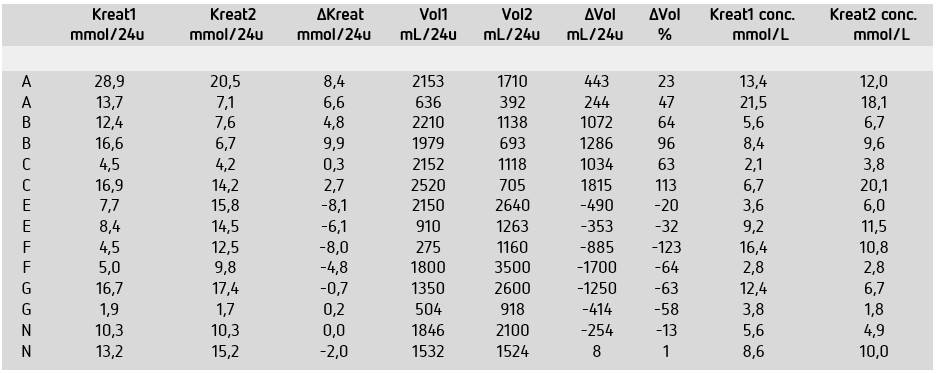
Urineverzamelingen werden als uitbijter benoemd als het verschil in de kreatinine-uitscheiding buiten ±4,0 mmol/24u of buiten ±40% lag, of wanneer het percentage volumeverschil buiten de ±55% lag. Op deze wijze vonden wij 63 uitbijters (23% van de populatie). Een selectie hiervan is weergegeven in Tabel 2. In de literatuur wordt de frequentie van in- of overcomplete verzamelingen zeer wisselend opgegeven, al naar gelang de diverse criteria voor detectie (bereik 6-47%, gemiddeld 20%) (4). Wij vonden 23% uitbijters, in goede overeenstemming met dit gemiddelde. In onze populatie signaleerde de absolute kreatinine-uitscheiding 39 uitbijters, de relatieve uitscheiding 37, en het relatieve volumeverschil slechts 18 uitbijters. In de analyse viel op dat geen van de 270 patiënten in de complementaire gebieden D of H viel (gebied D: Volume 1e etmaal >> 2e etmaal en Kreatinine-uitscheiding 1e etmaal << 2e etmaal). Kennelijk zijn deze combinaties extreem zeldzaam en ook minder waarschijnlijk in fysiologische zin en kunnen daardoor dienen als signalering van handmatige invoerfouten. In het gebied E viel een asymmetrie op: 18 patiënten lagen links van de Y-as en 5 patiënten rechts van de Y-as. Deze 18 patiënten hebben dus een verlaagd kreatinineverschil bij een normaal, negatief percentage volumeverschil (V2 > V1). Een dergelijke situatie kan ontstaan wanneer men de laatste portie van het 1e etmaal bij vergissing meeneemt in de verzameling van het 2e etmaal (zie verder onder Discussie).
Lage volumina
Bij 18 van de 63 patiënten was het 24-uurs volume in een of beide verzamelingen kleiner dan 1000 mL. Bij 11 patiënten van deze 18 leidde dit tot een afwijkend verschil in absolute kreatinine-uitscheiding, bij 12 patiënten in percentage kreatinine-uitscheiding en bij acht gevallen in percentage volumeverschil. In de literatuur wordt benadrukt dat bij lage volumina de tubulaire kreatininereabsorptie een grotere rol gaat spelen. Vaak worden deze patiënten dan ook uitgesloten bij het samenstellen van de onderzoekspopulatie. Hier is ervoor gekozen om deze gegevens toch in ons onderzoek te betrekken. Er kon geen verband worden gevonden tussen lage volumina en de ligging in een van de gebieden A t/m H.
Discussie
In het overzicht van Garde wordt de variabiliteit van de intra-individuele variatiecoëfficiënt van de 24-uurs kreatinine-uitscheiding bij gezonden (spreiding 9-35%) en bij patiënten (spreiding 10-27%) weergegeven (3). De database van Ricos geeft als gemiddelde 11%, gebaseerd op acht studies (14). De literatuur laat echter ook zien dat bij nauwgezet verzamelen een zeer kleine variatie haalbaar is: 3,6% (8). Dit roept de vraag op in hoeverre duidelijke patiëntinstructie en –motivatie een rol speelt. In het hiernavolgende onderdeel geven we een overzicht van vaak genoemde stoorfactoren op de kreatinine-uitscheiding.
Factoren van invloed op de variatie
Volume
In de literatuur wordt het gemiddelde (door patiënten geschat) gemiste volume opgegeven als 322 mL (frequentie 22%) (3) en 280 mL (frequentie 11%) (15). Een andere literatuurbron vermeldt bij niersteenpatiënten een gemiddeld volumeverschil tussen beide etmalen van +385 mL (16). Dit is een onverwachte systematische bias met een groter volume in het 1e etmaal.
Bij onderzoek naar het volume van de urineblaas is gebleken dat gezonde personen hoeveelheden van 120-465 mL urine (17), respectievelijk 45-508 mL (18) loosden. Opvallend is de brede spreiding van het geloosde volume. Wanneer men als voorbeeld een gemist volume van 300 mL bij een gemiddeld 24-uurs volume van 1700 mL aanneemt, is het verschil in volumepercentage 300/1700 = 18%.
Een heel denkbare vergissing zou kunnen zijn dat een patiënt bij het verzamelen in het 1e etmaal, de laatste portie niet meeneemt maar per abuis bij de 2e verzameling voegt. Hierdoor wordt het eerste volume te laag en het tweede te hoog en verdubbelt het percentage verschil naar -36%. Als gevolg hiervan stijgt het verschil in kreatinine-uitscheiding parallel mee en komt de patiënt daardoor in gebied E te liggen, en bij hogere volumeverschillen zelfs in gebied F. In onze metingen vinden we dit terug: de twee patiënten in het gebied F hadden een volumeverschil van 885 en 1700 mL; bij de patiënten in het gebied E lag dit tussen 100 en 796 mL.
In een andere situatie waarbij de patiënt de ochtendportie aan het eind van het 2e etmaal per abuis weggooit, hebben we de omgekeerde situatie, met een kleiner invers effect op het volumeverschil van +18%. Bij een laagnormale kreatinine-uitscheiding ligt de patiënt dan in gebied N, bij een hoognormale kreatinine-uitscheiding in gebied A, en bij een hoognormale kreatinine-uitscheiding in combinatie met een hoger volumeverschil in gebied B. In onze metingen vinden we in het gebied A een kreatinine-uitscheiding 12,9-28,9 mmol/24u; in het gebied B is dit 12,3-19,9 mmol/24u. In het gebied B is het volumeverschil 700-1286 mL.
De totale patiëntenpopulatie laat een gemiddeld volumeverschil van 8 mL zien en een gemiddeld verschil in kreatinine-uitscheiding van -0,1 mmol/24u. Er is dus, over de hele populatie genomen, geen systematische bias tussen het verzamelen in beide etmalen. Dit in tegenstelling tot een studie bij niersteenpatiënten waar een volumeverschil van +385 mL werd gevonden en een verschil in gemiddelde kreatinine-uitscheiding van 2,5 mmol/24u (16).
Inspanning
Recent is het effect van acute inspanning op de kreatinine-uitscheiding gemeten in een groep jonge mensen. De gemiddelde kreatinineconcentratie steeg hierbij van 5,0 naar 9,2 mmol/L na fietsergometrie (onder belasting van 152 W gedurende 30 minuten op 80% van de maximale hartfrequentie) (19). Deze inspanning is echter buitengewoon zwaar voor ouderen met obesitas of hypertensie en daarom in onze patiëntengroep onwaarschijnlijk als bron van variatie. Ook patiënten met fracturen zullen niet geneigd zijn een dergelijke inspanning aan te gaan.
Vlees
Het effect van consumptie van vlees is eveneens onderzocht: 225g gekookt vlees levert een stijging op van slechts 1,6 mmol kreatinine/24u (20). Deze orde van grootte is later bevestigd door andere auteurs (21,22).
Menstruatie
Het moment in menstruatiecyclus blijkt niet van invloed te zijn op de kreatinine-uitscheiding (23).
Kreatine
Inname van 20 g/dag kreatine verhoogt de kreatinine-uitscheiding acuut met circa 6 mmol/24 uur (24). In de chronische situatie is de verhoging slechts 2,8 mmol/24 uur. Om een verschil in kreatinine-uitscheiding op te kunnen leveren zou dit supplement precies voor het 2e etmaal moeten worden ingenomen, hetgeen tamelijk onwaarschijnlijk is.
Het is soms gebruikelijk om diverse analyten in 24-uurs urine als ratio ten opzichte van kreatinine uit te drukken. In de literatuur is benadrukt dat dit alleen kan als het analyt zich gedraagt zoals kreatinine (glomerulaire filtratie en tubulaire secretie) (25) en er geen spierafbraak is. Wij hebben in deze studie laten zien dat de 24-uurs uitscheiding van kreatinine van een patiënt binnen twee etmalen tot 4 mmol/24 uur kan verschillen. Deze variatie draagt extra bij aan de variatie in de berekende ratio. Wanneer men de voorkeur geeft aan rapportage als uitscheiding per 24 uur is het van belang om alles in het werk te stellen om een correcte verzameling te bewerkstelligen. Dit betekent een glasheldere patiëntenfolder en bijbehorende instructie.
Conclusie
Deze studie kent als zwakke punten het ontbreken van een gouden standaard voor urine verzamelen, die overigens nog steeds niet bestaat; verder waren de patiëntgegevens niet steeds in volledigheid beschikbaar. Sterke punten van deze studie worden gevormd door de grote patiëntengroep. Bij ons beste weten betreft dit onderzoek het grootste aantal patiënten gepubliceerd tot dusver, waarbij twee verzamelingen binnen 48 uur werden gespaard. Verder is er een gestandaardiseerde aanpak voor autorisatie gepresenteerd met duidelijke referentiegrenzen, die eenvoudig te automatiseren is.
De gegevens laten zien dat er in onze populatie geen systematische bias bestaat tussen beide verzamelingen. Ook zijn enkele storingsfactoren gekwantificeerd waardoor de orde van grootte beter op waarde geschat kan worden. We hebben tevens geconstateerd dat ten behoeve van een juiste dubbele verzameling onze patiëntfolder verbetering behoeft.
Door naar de relatie tussen het verschil in kreatinine-uitscheiding en het verschil in volume te kijken waren we in staat een model te ontwikkelen dat in de klinische praktijk gebruikt kan worden voor de detectie van relevante afwijkingen in 24-uurs urineverzamelingen. Concluderend kunnen we zeggen dat de bovengenoemde bekende storingen op de kreatinine-uitscheiding hetzij zeer meevallen qua orde van grootte ten opzichte van onze referentiegrenzen, hetzij onwaarschijnlijk zijn als stoorfactor in onze patiëntenpopulatie. Dit nodigt uit tot de conclusie dat de voornaamste bron van storing wordt gevormd door een verkeerde verzameling door de patiënt. Onze observatie van de asymmetrie in het gebied E sluit hierbij aan; het is echter geen definitief bewijs. Naar aanleiding van deze conclusie hebben we onze instructie voor de patiënt onder de loep genomen en geconstateerd dat deze een enkelvoudige 24-uurs verzameling weliswaar adequaat beschrijft, maar niet voldoende duidelijkheid geeft voor de handelwijze bij een dubbele 24-uurs verzameling. We hebben de tekst van deze folder inmiddels hierop aangepast.
Dankbetuiging
We zijn onze dank verschuldigd aan dr. S. Kos voor het kritisch lezen van het manuscript en het geven van opbouwende suggesties.
De auteurs verklaren geen potentiële belangenverstrengeling te hebben met betrekking tot het onderzoek, auteurschap en/of publicatie van dit artikel. De auteurs ontvingen geen financiële ondersteuning voor het onderzoek, auteurschap en/of publicatie van dit artikel. Ethische goedkeuring is niet noodzakelijk vanwege het gebruik van geanonimiseerde gegevens.